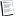
Đối với những phản ứng có chất khí tham gia, ngoài cách biểu diễn hằng số theo Kc, ta có thể biểu diễn hằng số cân bằng theo Kp.
Tổng quát:
aA(k) + bB(k) = cC(k) + dD(k), Kp
Kp = pC^c . pD^d : pA^a : pB^b
Với pA, pB, pC, pD là áp suất riêng phần của A,B,C,D ở trạng thái cân bằng.
Áp suất riêng phần của khí A là: pA = nA : nbình * ptổng
VD: Cl2 (k) ---> 2Cl (k)
Giả sử số mol Cl2 ban đầu là 1 mol.
Gọi độ phân ly của Cl2 thành Cl nguyên tử là x
Ta có: Cl2 (k) ---> 2Cl (k)
Ban đầu: 1mol
Lúc cân bằng: 1-x mol 2x mol
Ta có:
pCl = nCl : ntổng * ptổng = 2x : (1 - x + 2x) * ptổng
pCl2 = nCl2 : ntổng * ptổng = (1-x) : (1 - x + 2x) * ptổng
Kp = pCl^2 : pCl2
khi đã cho biết áp suất và độ phân ly ta có thể dễ dàng tính được Kp.
Xét cân bằng: aA(k) + bB(k) = cC(k) + dD(k)
Có các hằng số cân bằng là Kc, Kp, Kx và n = c + d - a - b
khi đó:
Kp = Kx*p^n = Kc*(RT)^n
Với p là áp suất tổng của phản ứng thực hiện ở nhiệt độ T
R là hằng số = 8,314 J:mol:K = 0,082 atm:mol:K = 1,987 Cal:mol:K (Cái này nhớ ko rõ)
Nhận xét: Với n=0 có thể thấy rằng Kp = Kx = Kc
thay đổi nội dung bởi: lopads1994, ngày 01-06-2010 lúc 10:40 AM.
|



